衛福部研發技術成果快訊 -- 膠質母細胞瘤創新療法:IL-19抗體雙效調控免疫抑制與腦水腫
2000-05-11技術名稱
膠質母細胞瘤創新療法:IL-19抗體雙效調控免疫抑制與腦水腫
計畫團隊 /
- 臺北醫學大學醫學院微生物與免疫學科 李爾博 副教授
- 臺北醫學大學醫學院放射線學科 陳震宇 教授
- 臺北醫學大學生藥學研究所 莊國祥 教授
- 臺北醫學大學醫學科學研究所 張育維 博士生
- 臺北醫學大學事業發展處 吳旭倍 主任
技術摘要
本技術針對膠質母細胞瘤(glioblastoma, GBM)中關鍵免疫抑制因子 IL-19,藉由IL-19抗體治療可重塑腫瘤免疫抑制微環境、提升CD8⁺ T細胞活性,進而抑制腫瘤生長與侵襲。相較現有療法,本技術可同時改善腫瘤免疫抑制與腦水腫問題,並已證實可與VEGF-A抗體產生協同效果,可加強降低血管滲漏與抑制腫瘤生長之效果。此技術具first-in-class潛力,可作為單一療法或與現行治療併用,具高度臨床轉譯與技術授權價值。
技術內容
本技術聚焦於膠質母細胞瘤(glioblastoma, GBM)長期未被有效解決的兩大核心臨床挑戰:腫瘤免疫抑制微環境與腫瘤相關腦水腫。目前標準治療(手術、放射治療與化學治療)以及抗血管生成療法(如VEGF-A抗體)雖可暫時控制腫瘤進展,然而對整體存活期的改善仍有限;此外,腦水腫治療仍主要依賴類固醇,長期使用易導致顯著副作用,臨床需求尚未被滿足。
本技術以IL-19作為創新治療標的,透過IL-19抗體介入,從「免疫調控」與「血管/水分調控」兩大面向,同步改善腫瘤免疫抑制與腦水腫問題,具備雙效治療潛力。
一、重塑腫瘤免疫微環境並抑制腫瘤侵襲
1.抑制腫瘤生長(涵蓋TMZ敏感與抗藥性GBM)
IL-19抗體可有效抑制temozolomide(TMZ)敏感與抗藥性GBM腫瘤生長。
2.解除免疫抑制微環境
阻斷IL-19訊號可降低M2型腫瘤相關巨噬細胞(tumor-associated macrophages, TAM)之免疫抑制功能,並下調免疫抑制相關基因(如Arg1、CD274),進而恢復CD8⁺ T細胞活性,重塑抗腫瘤免疫反應。
3.抑制腫瘤遷移與侵襲
透過干擾IL-19/WISP1訊號軸,降低GBM細胞的遷移與侵襲能力,進一步抑制腫瘤惡性進展。
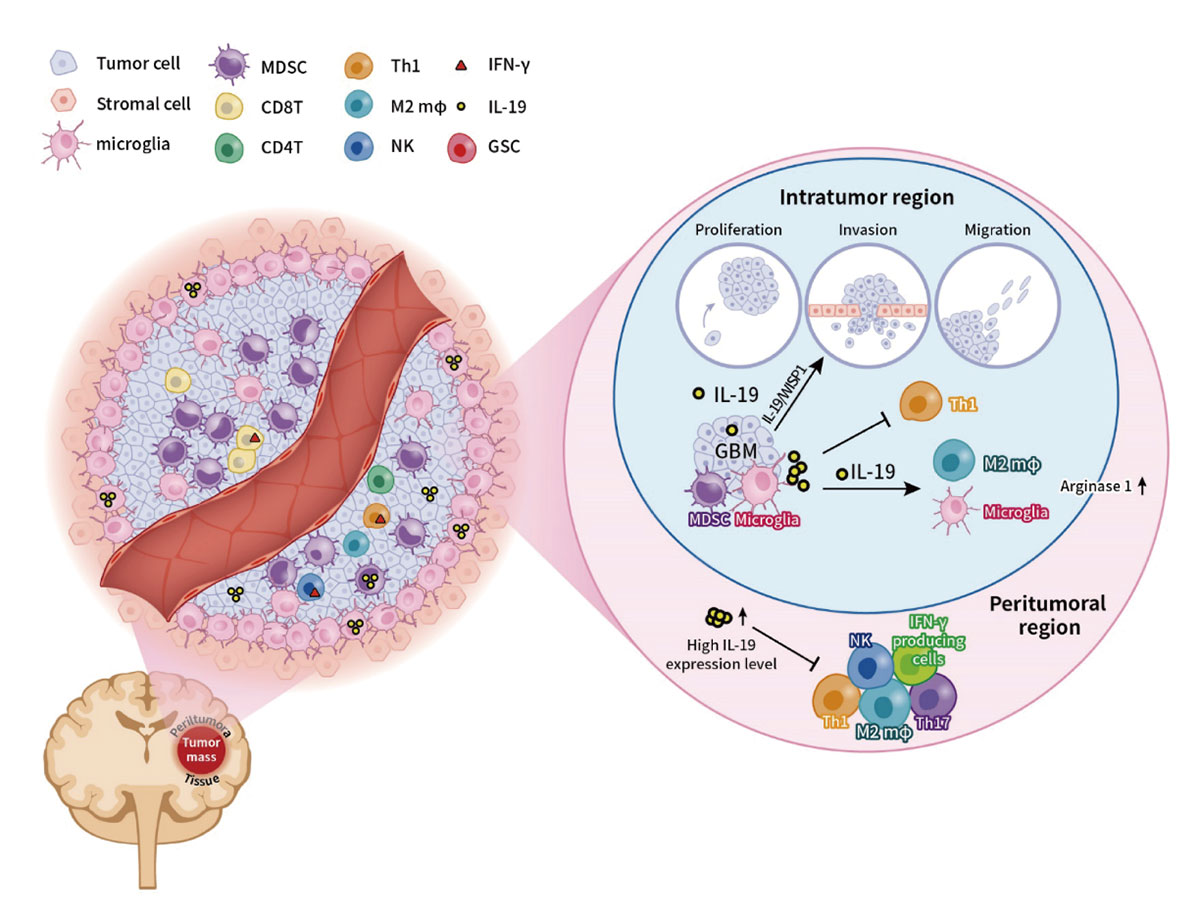
圖1.IL-19在膠質母細胞瘤(GBM)腫瘤微環境中的角色。
IL-19抗體治療可延長GBM腫瘤小鼠的存活期。GBM細胞、骨髓來源抑制性細胞(MDSCs)以及腫瘤浸潤的小膠質細胞皆表現IL-19。IL-19透過WISP1/AKT訊號途徑促進腫瘤細胞的增殖、侵襲與遷移。IL-19抑制TH1型免疫反應,並促進M2巨噬細胞及小膠質細胞中Arg1的表現。
二、雙重機制改善腦水腫
IL-19抗體可同時調控「血管滲漏」與「水分運輸」兩條關鍵路徑,有效抑制腫瘤相關腦水腫:
1.抑制腫瘤VEGF-A表現而降低血管通透性:減少異常血管新生與通透性,從源頭抑制液體外滲。
2.抑制腫瘤水分子通道表現:抑制腫瘤細胞水通道蛋白(AQP1)的表現,減少水分跨細胞運輸與組織積水。
3.與VEGF-A抗體治療具協同作用:與VEGF-A抗體療法併用時,可進一步降低腫瘤體積與血管滲漏,顯著改善腫瘤周邊水腫,展現協同治療潛力。
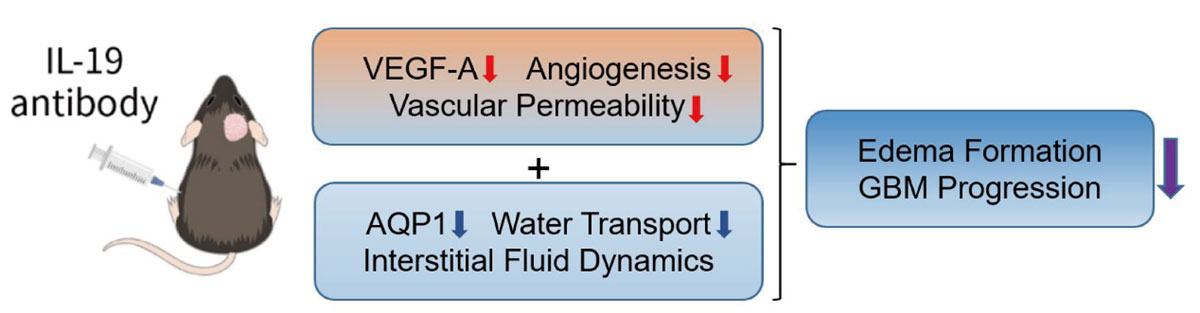
圖2.IL-19抗體透過調控血管通透性與水分運輸來抑制腦水腫形成。
IL-19抗體治療可降低VEGF-A表現,進而抑制血管新生與血管通透性。同時,也可以下調AQP1表現,減少水分運輸及間質液體動態。上述機制共同作用,最終有效抑制腦水腫。
本技術透過IL-19抗體實現「免疫重塑 × 腦水腫控制」的雙效治療策略,為GBM提供具臨床轉譯潛力的創新解決方案。
技術優勢與亮點
- First-in-class標的
IL-19為尚未被開發的免疫抑制關鍵細胞激素,具專利佈局空間。 - 精準免疫調控(Precision Immunomodulation)
不同於checkpoint inhibitors,本技術直接針對腫瘤微環境調控,副作用風險較低。 - 雙重臨床效益(腫瘤+腦水腫)
同時解決腫瘤進展與腦水腫,為目前市場技術缺口。 - 高度併用潛力(Combination-ready asset)
可與VEGF-A抗體、化療或放療併用,提高既有療法價值。 - 抗藥性適用(TMZ-resistant有效)
具突破現行治療抗藥性之潛力。
團隊簡介或技術聯絡人
臺北醫學大學醫學院微生物與免疫學科
李爾博 副教授
E-mail:gilbertlee@tmu.edu.tw
電話:0958880131
